Die Wirkung von QRS auf den menschlichen Alterungsprozess
Hintergrund
Zellen können sich im Laufe unseres Lebens nicht unendlich teilen und erneuern, sondern besitzen eine natürliche Erneuerungsgrenze [1]. Die Teilungsgrenze unterscheidet sich je nach Zellentyp voneinander. Stammzellen sind von der Begrenzung allerdings weniger betroffen [2]. Die zelluläre Teilungsgrenze wirkt sich vor Allem auf die Regenerationsfähigkeit verletzten oder geschädigten Gewebes oder Organen aus und birgt ein erhöhtes Risiko für gesundheitliche Probleme, die mit dem Alterungsvorgang verbunden sind [3].
Alte bzw. verbrauchte Zellen werden vom Immunsystem eliminiert. Doch auch das Immunsystem unterliegt dem Alterungsprozess. So kommt es im Laufe des Älterwerdens zu einer Anhäufung gealterter Zellen [4]. Diese setzen einen Cocktail von Enzymen und Signalsubstanzen wie z.B. Matrix-Metalloproteinasen (physiologische Funktionen in Prozessen) frei, welche die extrazelluläre Matrix (Gewebe im Bindegewebe) angreifen bzw. Entzündungsreaktionen fördern.
Wir konzentrieren uns in dieser Ausarbeitung auf epigenetische, mitochondriale, zelluläre, sowie auf physiologische Abläufe und weniger auf die äusserliche Antiaging-Medizin. Gleichwohl dazu ebenso interessante Erkenntnisse bestehen, z.B. der Nachweis von Rejuvenationseffekten (Effekt der Hautverjüngung), die jedoch aus medizinischer Sicht in dieser Ausarbeitung weniger Relevanz haben.
Einen ernsthaften, wissenschaftlich-biophysikalischen Nachweis der Wirkung von QRS auf den Alterungsprozess zu erbringen, erfordert die jeweiligen „Einzelprozesse“ und Einflussfaktoren mit dem QRS-Wirkmodell abzugleichen. Nachfolgend erläutern wir die Einflussnahme von QRS auf die einzelnen Faktoren, die bei der Alterung – in Bezug auf die Zellprozesse – im Wesentlichen zu berücksichtigen sind. Selbstverständlich ist vorbeugen, besser als heilen, jedoch kann QRS auch die Therapie bestehender Problematiken unterstützen.
Einfluss von QRS auf die Durchblutung
QRS wirkt direkt am Gefässsystem, was sich sowohl in der Angiogenese (Wachstum von Blutgefässen) [5], als auch in einer Verstärkung der Kapillardurchblutung (Durchblutung feinster Verzweigungen der Blutgefässe) zeigt. Dahinter „steckt“ eine QRS-stimulierte Stickstoff-Monoxid (NO)-Bildung in den kleinen Blutgefässen [6], was auch damit zu tun hat, dass NO natürlicherweise die Blutflussregulation bestimmt [7].
Der Background zu dieser Physiologie wurde durch das neue Magnetstimulationsverfahren QRS rPMS (QRS Pelvicenter) „aufgedeckt“. Die (hochintensive) repetitive periphere Magnetstimulation besitzt eine Reihe gemeinsamer Basiseigenschaften mit der (niederintensiven) klassischen QRS-Magnetfeldtherapie.
Festgestellt wurde, dass es zu einer magnetfeldinduzierten NO-Erhöhung über einen Anstieg des Enzyms eNOS (endotheliale Stickstoffmonoxid-Synthetase) kommt [8].
Mit der in diesem Zusammenhang bedingten Entspannung der glatten Gefässmuskelzellen, erweitern sich endothelausgekleideten Arteriolen (kleinste Arterien, die den mikroskopisch dünnen Kapillaren vorgeschaltet sind), was umso bedeutsamer ist, weil der sich ergebende, erhöhte Blutdurchfluss nach einer QRS Anwendung für min. 3 Std. nachweislich erhalten bleibt [9],[10].
Damit einhergehend verbessern sich die Fliesseigenschaften des Blutes, weil eNOS auch eine Thrombozyten-Aggregationshemmung (Zusammenlagerung von Blutplättchen) bewirkt. Zudem „befeuert“ ein resultierender Anstieg des Signal-Moleküls AKT (Proteinkinase B) und von VEGF (Vascular Endothelial Growth Factor) die Angiogenese (Wachstum von Blutgefässen) [11],[12]. Eine QRS-stimulierte Angiogenese erfolgt auch durch den endothelialen Wachstumsfaktor FGF-2 (Prozesssteuerung der Angiogenese) [13].
Durch das mikrozirkulationssteigernde und angiogenetische Thrombozytenaggregations-Potential (Aspirin-Effekt) kann QRS die schleichende Entwicklung von „klinisch stummen“ Durchblutungsstörungen verhindern oder zumindest reduzieren. Somit ist die Prävention altersbeeinflussender Degenerationsvorgänge, wie z.B. die einer Arteriosklerose und ihrer Begleiterkrankungen möglich.
Einfluss von QRS auf die Zellspannung
Eine optimale Zellspannung (bzw. Membranpotential) „kontrolliert“ direkt oder indirekt die Wundheilung [14],[15],[16],[17] und fördert die Zellregeneration [18]. Aus der QRS Literatur der Magnetstimulation ist bekannt, dass mit einem elektromagnetisch induzierten Feld eine Spannung an der mitochondrialen Zellmembran entsteht [19]. Dies führt zu einigen physiologischen / „pathologischen“ Veränderungen, wie z.B. einer Öffnung des mitochondrialen Poren-Komplex [20].
QRS kann das zelluläre Membranpotential erhöhen, wobei dieser Effekt sowohl auf den Erkenntnissen zur zellulären „Abwehrreaktion“, als auch auf den Ergebnissen einer Pilotstudie zur Mikrostromtherapie beruht. Mit einer Zunahme des Membranpotentials offenbart sich durch QRS ein nennenswertes Vitalitäts- und Vigilanzpotential (Aktivierung des Nervensystems).
Einfluss von QRS auf die Zellkraftwerke
Der Grund, warum durch ein körperliches Ausdauertraining die Ausdauerleistung steigt, liegt daran, dass muskuläre Aktivität die intrazelluläre Ca++ Konzentration erhöht, welches wiederum die Ca-Calmodulin-abhängige Proteinkinasen (CaMK) aktiviert [21]. Damit wird eine gesamte Reaktionskette in Gang gesetzt, an deren Ende sich die Anzahl der Mitochondrien (ATP-Energieproduzenten innerhalb der Zelle) dauerhaft erhöht [22],[23]. Dementsprechend besitzen sportliche Personen mehr Mitochondrien in ihren Muskelzellen als unsportliche und haben zudem wegen der im Zusammenhang stehenden, erhöhten ATP-Produktion eine bessere Kondition.
Durch eine QRS-Magnetfeldstimulation kann nach dem Prozessketten-Prinzip durch körperliche Bewegung, das intrazelluläre Ca++ erhöht werden. In der Folge sind die gleichen, positiv anregenden Stimulationseffekte auf die mitochondriale Reduplikation zu erwarten, die zwar geringer ausfallen als durch eine bewegungsbedingte Belastungssituation, sich jedoch im messbaren und am möglichen Therapieerfolg beteiligten Bereich befinden.
Einfluss von QRS auf die Energieproduktion
Das grundlegende Prinzip des QRS-Systems führt grundsätzlich zu einem erhöhten Ionen-Andrang an den Grenzflächen der äusseren Zellmembran (Int. QRS-Patent zum Transport von Ionen) und erhöht damit die Leckströme (ionischer Strom, der bei Nervenzellen im Ruhezustand durch offene Kaliumkanäle fliesst) in Richtung Cytosol (Natrium). Davon ist zudem der Kalium-Kanal betroffen, so dass weniger Kalium-Ionen nach aussen driften.
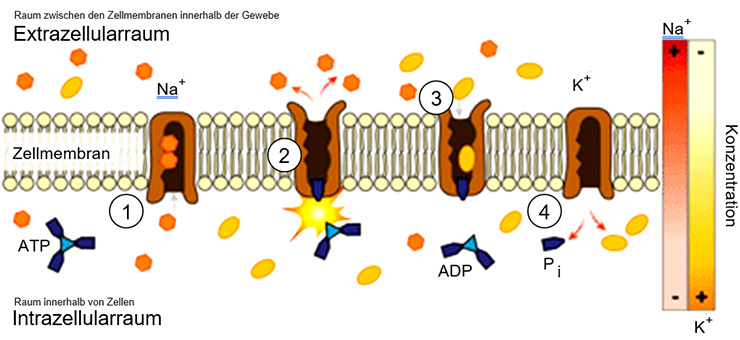
Grafik: (1) Die Natrium Kalium Pumpe ist zu Beginn nur dem Zellinneren zugewandt und auch nur für diese Seite offen. In der Ionenpumpe befinden sich spezielle Carrierproteine (Befördererproteine) an denen nur Kalium und Natrium Ionen andocken können. Die Carrierproteine für Kalium sind in dem Moment, wo die Ionenpumpe zum Intrazellulärraum hin geöffnet ist, aber deaktiviert. So können nur Natrium Ionen an die drei Bindungsstellen andocken. (2) Wenn alle gleichartigen Carrierproteine besetzt sind, klappt der Mechanismus der Pumpe um, wodurch sich die Ionenpumpe zum Extrazellularraum hin öffnet und zum Intrazellularraum hin schliesst. Durch diesen Mechanismus stellt die Zelle sicher, dass wirklich nur ihre beförderten Ionen die Membranseite wechseln. (3) Der Prozess wiederholt sich jetzt mit Kalium: An den zwei Andockstellen der Carrierproteine lagern sich die Kalium Ionen an. (4) Der Mechanismus klappt wieder um und gibt die beiden Kalium Ionen ins Zellinnere frei.
Es kommt zum Abfall des zellulären Membranpotentials, was als Gegenreaktion einen Verschluss der Ionenkanäle zur Folge hat. Gleichzeitig versuchen die Ionenpumpen, den Membranpotential-Sollwert wiederherzustellen.
Das Ergebnis ist als Reaktion der Zelle zu verstehen, welche eine Umstellung von der anaeroben in die aerobe Energieherstellung erzwingt: Der erhöhte Energiebedarf für die Ionenpumpen, die bereits in Ruhe min. 40% der zelleigenen ATP-Produktion (Adenosintriphosphat, Energieproduktion) entspricht, beginnt die sofortige (innerhalb 60 Sek.) Umrüstung von der anaeroben (wenig Sauerstoff) auf die aerobe (viel Sauerstoff) Energieherstellung.
Da sowohl die Ionenpumpen, also auch die mitochondriale Energieerzeugung immer in einem zeitlich überlappenden „Modus“ arbeiten (20 bis 30 Min.), entsteht nach einer QRS-Sitzung immer eine höheres Membranpotential (Zellspannung) und ergibt sich eine höhere Verfügbarkeit von ATP während der QRS-Anwendung.
QRS besitzt das grundsätzliche Initialmoment einer aeroben Energieanforderung, mit der Folge einer nachfolgenden erhöhten mitochondrialen ATP-Energieproduktion. Sämtliche zelluläre Reaktionen setzen ein „Zellmanagement“ in Gang, weshalb eine mittel- bis langfristige QRS-Therapie prinzipiell zu einem positiven Ergebnis führen kann.
Einfluss von QRS auf das Stresssystem
Die oxidative Schädigungstheorie (Schädigung durch überschreitende Mengen reaktiver Sauerstoffverbindungen) sagt aus, dass freie Sauerstoffradikale, die hauptsächlich als „Nebenprodukt“ in Form von ROS (Reactive Oxygen Species) innerhalb der aeroben Energieerzeugung entstehen (weitere Quellen sind Umweltgifte, Abgase oder z.B. Zigarettenrauch), Zellmembrane und den Zellkern schädigen und so die Alterung beschleunigen und die Lebenszeit verkürzen [24].
Auf molekularer Ebene kann QRS den intrazellulären Redox-Status (Elektronenübertragung) positiv beeinflussen [25], womit die Expression (Informationsrealisierung) stressbezogener Proteine gefördert wird [26]. Während sich durch eine einzelne QRS-Applikation die ROS erhöhen, nimmt der ROS-Level nach wiederholten Anwendungen (> 3) deutlich ab [27]. Hypersensible Personen bemerken die ROS-Erhöhung bei der QRS-Erstanwendung evtl. durch eine leichte Verschlechterung der Symptomatik, die sich jedoch bereits ab der 2. Anwendung normalisiert.
Man interpretiert diese mögliche Reaktion als eine Stimulation körpereigener antioxidativer Verteidigungsmechanismen, dem „Hormesis-Prinzip“, das bei der Membranpotential- und ATP-Erhöhung nach QRS eine wichtige Rolle spielt. Eine Aktivierung des körpereigenen, antioxidativen Abwehrsystems bzw. verminderter ROS nach QRS wird durch Studien bestätigt [28],[29].
Einfluss von QRS auf die Herzratenvariabilität
Eine 20-minütige QRS-Sitzung kann die Herzratenvariabilität (HRV) verbessern [30], was um so bedeutender ist, weil die HRV als das Mass für eine gute vegetative Regulationsfähigkeit gilt. Aus einer Untersuchung zu unterschiedlichen Einstellparametern (Intensität) ging z.B. hervor, dass eine QRS-Anwendung vorwiegend auf den Sympathikus wirkt [31].
So zeigte sich in der HRV-Bestimmung, dass sich die VLF (Very Low Frequencies), die für den Sympathikus stehen, nach einer vorherigen Stress-Exposition unter QRS schneller erholten als die Placebo-Gruppe. Insgesamt führte hier eine 20-minütige QRS-Anwendung zu einer Verbesserung der HRV.
HRV ist auch ein zentraler Marker zur Bestimmung von Performance und Vigilanz (Wachsamkeit) [32]. Dabei ist eine Verschlechterung der Vigilanz sehr eng mit Änderungen des autonomen Nervensystems verbunden, welches sehr empfindlich auf innere Anforderungen und äussere Einflüsse reagiert. In einer HRV-kontrollierten Studie führte eine QRS-Anwendung – im Vergleich zur Kontrollgruppe – zu einer signifikanten Verbesserung der Vigilanz [33].
Einfluss von QRS auf den Schlaf
Ausreichend Schlaf hat einen hohen Einfluss auf ein gesundes und langes Leben, bzw. andersherum kann zu wenig Schlaferholung zu erheblichen körperlichen und gesundheitlichen Störungen führen, die sich auch auf die Lebenserwartung niederschlagen kann.
In einer evidenzbasierenden Studie, wurden insgesamt 101 Patienten mit Schlafstörungen (Einschlafprobleme, Durchschlafprobleme und Albträume) über 4 Wochen mit dem QRS-System behandelt [34]. Überprüft wurden die Parameter Einschlafzeit, Anzahl der Schlafunterbrechungen, Schläfrigkeit nach dem Aufstehen, Tagesmüdigkeit, Konzentrationsstörungen sowie Tages-Kopfschmerzen.
Die doppelblinde, placebokontrollierte Schlafstudie hat ergeben, dass 70% der QRS-Gruppe eine Verbesserung ihrer Schlafproblematik erfahren haben: 24% berichteten über eine deutliche, 40% über eine teilweise und 6% über eine leichte Verbesserung.
Einfluss von QRS auf Stammzellen
Stammzellen sind in allen Geweben von Säugetieren vorzufinden und dienen der Regeneration und Reparatur nach Verletzungen und der Selbsterneuerung. Die diesbezügliche QRS-Wirkung ist vor allem in einer leichten Erhöhung der Stammzell-Proliferation zu suchen [35],[36],[37],[38].
Isolierte und kultivierte Stammzellen werden bereits zur Behandlung von Erkrankungen des Herzens [39], der Leber [40],[41],[42],[43] oder auch bei neurogenerativen Krankheiten eingesetzt [44]. Z.B. führt eine Studie unter spezifischen Frequenz-Settings des Magnetfeldes zur Neurogenese im Hippocampus (Bildung von Nervenzellen im limbischen Gehirnteil) von erwachsenen Mäusen, dem Ort wo die Langzeitspeicherung von Gedächtnisinhalten stattfindet [45].
Mit einer 14- und 28-tägigen QRS-Anwendung unter Studien-spezifischen Settings kam es im Tierversuch zu einer wachsenden Zunahme der demyelinisierten Areale (Re-Myelinisierung), wobei sich der Level von MBP (Myelin Basic Protein) sowie der BrdU- und Nestin-positiven Stammzellen erhöhte.
Dies weist darauf hin, dass QRS die Proliferation (Wachstum und Teilung) und Migration (Wanderung) neuronaler Stammzellen (Vorläufer der Nervenzellen) potenzieren und damit die Myelinreparatur (Reparatur der Faserisolierschicht) verbessern kann [46].
Zur elektromagnetisch pulsierenden Stimulation von Stammzellen gibt es eine Reihe von Invitro-, aber auch Invivo-Studien (Tierversuch), welche die immense Bedeutung für eine mögliche Zellerneuerung deutlich unterstreichen.
QRS kann die Proliferation (Wachstum und die Vermehrung) von Stammzellen stimulieren. Ob hier epigenetische Mechanismen eine Rolle spielen, ist dabei sekundär. Auf jeden Fall lässt sich dieses Potential auf sämtliches Gewebe übertragen, nachdem sich die aktuelle Studienlage nicht nur auf die Gewebsreparatur und Wundheilung nach Verletzungen, sondern allgemein auch auf Neuronen des ZNS (Zentrales Nervensystem) und der Knochen- und Knorpelbildung bezieht.
Einfluss von QRS auf die Frakturheilung / Pseudarthrosen / Osteoporose-Prophylaxe
Die Frakturheilung / Pseudarthrosen [47],[48] sowie die Osteoporose-Prophylaxe und deren Therapie [49],[50],[51],[52],[53] zählen zu den Haupteinsatzgebieten von QRS. So konnte eine Proliferation und Mineralisation der Osteoblasten, bei gleichzeitiger Hemmung der Osteoklastengenese, festgestellt werden [54],[55],[56]. Auch eine Stimulation der Chondrozytenproliferaton wurde beobachtet [57].
Dies geschieht wegen der piezoelektrischen Eigenschaften (Elektrische Spannung durch Bewegung/Verformung) der kollagenen Matrix (Strukturproteine) und elektrokinetischen Effekten („streaming potentials“), nachdem natürliche Bewegungen verbunden mit mechanischen Belastungen der Knochen elektrische Potentiale entstehen lassen [58],[59],[60]. Der gleiche Effekt kann durch QRS grundsätzlich dadurch simuliert werden, weil das QRS-System auf piezoelektrischen Eigenschaften (schieben und ziehen von Ionen) beruht [61].
Einfluss von QRS auf elektromagnetische Rezeptoren
Durch elektromagnetische „Reizung“ (Besetzung) zellulärer, elektromagnetisch reagierender Membran-Rezeptoren (Signalempfänger) kommt es zur Bildung von Botenstoffen (Signalübertragungsstoffe), die als sog. Second messengers (z.B. cAMP und Ca++) für fast alle Zellaktionen verantwortlich sind [62],[63], wobei zwischen metabotropen („Rezeptor reicht bis in die Zelle und setzt sekundären Botenstoff frei“) und ionotropen Rezeptor („öffnet einen Ionenkanal“) zu unterscheiden ist. Auch Transmembranrezeptoren, die auf die elektromagnetische „Reizung“ reagieren (Parathormon, Insulin, Transferrin oder Calcitonin) werden aktiviert, die in einer Signalkaskade (über mehrere Stationen laufendes biologisches Signal) enden [64].
Wichtig ist auch die Proteinkinase ERK (Regulation im Energiestoffwechsel), da der ERK-Signalweg wichtige Zellfunktionen wie die Proliferation (Wachstum / Vermehrung) und Differenzierung (Zell- oder Gewebsentwicklung) steuert. ERK kann durch verschiedene extrazelluläre Signale sowie QRS-bedingt, elektromagnetisch durch die Signaltransduktion (Signalübertragung) aktiviert werden [65],[66]. Über die ERK1/2-Signalkaskade kann eine erhöhte QRS-bedingte mitochondriale Aktivität im Knochengewebe nachgewiesen werden [67].
Zusammenfassung
Unter Berücksichtigung der wesentlichen Einflussfaktoren des Alterungsvorgangs existieren Studiennachweise, die einen altersbeeinflussenden positiven Effekt durch das QRS-System bestätigen.
QRS kann zelluläre Abbauvorgänge hemmen, indem über die Botenstoffe cAMP und Ca++ eine Vielzahl von Wachstums- und Vermehrungsprozessen der Zell- und Gewebsentwicklung (Proliferations- und Differenzierungsprozesse) samt einer Mitochondrienvermehrung (Vermehrung der Zellkraftwerke) angestossen werden.
Das Ziel ist neben einem höheren Membranpotential ebenso eine höhere Energiegewinnung durch eine erhöhte ATP-Produktion zu erreichen. Nicht nur die universelle und unmittelbar verfügbare Energieversorgung, sondern auch die Regulation wichtiger energieliefernder Prozesse ist eine beabsichtigte Folgewirkung.
Zudem kann durch eine QRS-Stimulation von Kryptochromen (Bindung zellulärer Proteine) eine Synchronisierung der Genaktivität erfolgen. rRNAs (Umsetzung von genetischer Information in Proteine) stossen die für eine Zellerneuerung so wichtige Apoptose (programmierter Zelltod) an oder produzieren stimulierte Fibroblasten (Auf- und Abbau der Zwischenzellsubstanz) vermehrt Kollagen (Strukturproteine im Bindegewebe).
QRS kann das körpereigene antioxidative System aktivieren, was insoweit wichtig ist, als eine Supplementierung mit den antioxidativ wirksamen Vitaminen C und E die notwendige Proteinsynthese für den Muskelaufbau im Sport sowie den Knochenaufbau bei Älteren unterbindet, weshalb speziell für die Bekämpfung freier Radikale der Einsatz von QRS einer Vitamingabe (C+E) vorzuziehen ist.
Genauso, wie Lebenstil und soziale Interaktionen die epigenetische Methylierung (Ein- oder Ausschalten von Genen) beeinflussen können, kann dies im gewissen Masse und im positiven Sinne ebenso durch die QRS-Anwendung erfolgen. Zwar kann der Einfluss externer, epigenetischer Signale, wie sie durch QRS erzeugt werden, gegenüber der vererblichen Epigenetik („epigenetische Uhr“) nicht gleich hoch bewertet werden, jedoch machen die durch QRS erzielbaren Einflussmöglichkeiten einen – ausserhalb genetischer Prädisponierungen (genetisch bedingte Erkrankungsempfänglichkeit) – möglichen Antiaging- bzw. einen lebensverlängernden Effekt aus.
Unter QRS kann sich nachweislich die Herzratenvariabilität (HRV) verbessern, was einer Unterstützung der vegetativen Regulationsfähigkeit entspricht und somit einen förderlichen Einfluss auf das biologische Alter zur Folge haben kann.
Die QRS-Systeme QRS 101 Homesystem und QRS 310 Arztsystem verfügen über eine therapeutisch sinnvolle Varianzbreite, durch die ein berechtigtes Potential besteht, im Einflussgebiet des Alterungsvorgangs, zu einem gewissen Anteil – ohne negative Nebenwirkungen – eingreifen zu können. QRS kann einen Beitrag dazu leisten, ein längeres Leben, bei guter Gesundheit im Alter zu ermöglichen.
Quellen:
[1] Hayflick L, Moorhead PS. The serial cultivation of human diploid cell strains. Exp. Cell Res. 1961: 25:585-621
[2] Ho AD, Wagner W, Mahlknecht U. Stem cells and ageing. EMBO Rep. 8(Suppl ). S35-S38
[3] Hayflick L. How and why we age. New York. NY. USA. Ballantine Books. 1994
[4] Baker DJ, Childs BG, Durik M et al. Naturally occuring p16 Ink4a – positive cells shorten healthy lifespan. Nature. 2016; 530: 184-189
[5] Tepper OM, Callaghan MJ, Chang EI et al. Electromagnetic fields increase in vitro and invivo angiogenesis trough endothelial release of FGF-2. FASEB J. 2004; 18: 1231-1233
[6] Diniz P, Soejima K, Ito G. Nitric oxide mediates the effects of pulsed electromagnetic field stimulation on the osteoblast proliferation and differentiation. Nitric Oxide. 2002;7:18–23
[7] Chichon N et al. Benign effect of extremely low-frequency electromagnetic field on brain plasticity assessed by nitric oxide metabolism during poststroke rehabilitation. Oxid Med Cell Longev 2017: 2181942. doi: 10.1155/2017/2181942. Epub 2017 Sep 12
[8] Lee D. Beom J, OH BM et al. Effect of magnetic stimulation in spinal cord on limb angiogenesis and implication: a pilot study. Ann Rehabil Med. 2012; 36: 311-319
[9] Bragin DE et al. Increases in microvascular perfusion and tissue oxygenation via pulsed electromagnetic fields in the healthy rat brain. J Neurosurg 2015; 122(5): 1239-47
[10] Smith TL, Wong-Gibbons D, Maultsby J. Microcirculatory effects of pulsed electromagnetic fields. J. Orthop Res 2004; 22(1): 80-4
[11] Li RL, Huang JJ, Shi YQ. Pulsed electromagnetic field improves postnatal neovascularization in response to hindlimb ischemia. Am J Transl Res. 2015; 7(3): 430-444
[12] Choi MC, Cheung KK, Zhang Y et al. Can pulsed electromagnetic field (PEMF) be a potential treatment for promoting angiogenesis in diabetic brain. Physiotherapy. 2015; 101(1): e247
[13] Oren M, Tepper MJ, Callaghan EI et al. Electromagnetic fields increase in vitro and in vivo angiogenesis through endothelial release of FGF-2. The FASEB Journal express article10.1096/fj.03-0847fje. Published online June 18, 2004
[14] Jorgenson WA, Frome BM, Wallach C. Electrochemical Therapy of Pelvic Pain: Effects of Pulsed Electromagnetic Fields (PEMF) on Tissue Trauma, European Journal of Surgery, 1994, 574(Suppl.); 83-86
[15] Nucitelli R. Endogenous electric fields in embryos during development, regeneration and wound healing. Radiat Prot Dosimetry 2003; 106: 375-383
[16] Nuticelli R. A role for endogenous electric fields in wound healing. Curr Top Dev Biol. 2003; 58: 1-26
[17] McCraig et al. Electrical dimensions in cell science. J Cell Sci 2009; 122: 4267-4276
[18] Levin M. Large-scale biophysics: ion flows and regeneration. Trends Cell Biol. 2007; 17: 261-270
[19] Vajrala V, Claycomb JR, Sanabria H et al. Effects of oscillatory electric fields on internal membranes: an analytical model. Biophys J 2008; 94: 2043-2052
[20] Weaver J. Electroporation of Biological Membranes From Multicellular to Nano Scales. IEEE Trans Dielectr Electr Insul 2003; 10: 754-768
[21] Mairbäurl H. Regulation of Gene Expression in Muscles under Exercise. Deutsche Zeitschrift Sportmedizin. 2006; 57(3): 61-67
[22] Schultz RA, Swoap SJ, McDaniel LD et al. Differential expression of mitochondrial DNA replication factors in mammalian tissues. J Biol Chem. 1998; 273(6): 3447-3451
[23] Wu H, Kanatous SB, Thurmond FA et al. Regulation of mitochondrial biogenesis in skeletal muscle by CaMK. Science (New York, N.Y.). 2002; 296(5566): 349-352
[24] Harman D. Aging: a theory based on free radical and radiation chemistry. J Gerontol. 1956; 11: 298-300
[25] Goodman R, Blank M. Insights into electromagnetic interaction mechanisms,” J Cell Physiol, 2002192(1): 16-22
[26] Osera C, Fassina L, Amadio M et al., Cytoprotective response induced by electromagnetic stimulation on SH-SY5Y human neuroblastoma cell line. Tissue Engineering. 2011; 17(19-20) 2573–2582
[27] Ehnert S, Fentz AK, Schreiner A et al. Extremely low frequency pulsed electromagnetic felds cause antioxidative defense mechanisms in human osteoblasts via induction of •O2 − and H2O2. Sci Reports. 2017;7: 14544 | DOI:10.1038/s41598-017-14983-9
[28] Gözen H, Demirel C, Akan M et al. Pulsed electromagnetic field effects on antioxidant levels of diabetic rats. Eur J Ther. 2017; 23:152-158
[29] Lim S, Kim SC, Kim JY. Protective Effect of 10-Hz, 1-mT Electromagnetic Field Exposure Against Hypoxia / Reoxygenation Injury in HK-2 Cells. Biomed Environ Sci. 2015;28(3): 231–234
[30] Grote V, Lackner H, Kelz C et al. Short-term effects of pulsed electromagnetic fields after physical exercise are dependent on autonomic tone before exposure. Eur J Appl Physiol.2007; 101(4): 4956-502
[31] Grote V et al. Short-term effects of pulsed electromagnetic fields after physical exercise are dependent on autonomic tone before exposure. Eur J Appl Physiol 2007; 101(4): 495-502
[32] Chua EC, Tan WQ, Yeo SC. Heart rate variability can be used to estimate sleepiness related decrements in psychomotor vigilance during total sleep deprivation. Sleep 2012; 35(3): 325-334
[33] Cui H et al. Effects of magnetic stimuli on vigilance: a heart rate variability analysis. JPBS 2017; 2(3): 1
[34] Pelka RB, Jaenicke C, Gruenwald J. Impulse magnetic-field therapy for insomnia: a double-blind, placebo-controlled study. Adv Therapy 2001; 18(4): 174-80
[35] Gaetani R, Ledda M, Barile L et al. Differentiation of human adult cardiac stem cells exposed to extremely low frequency electromagnetic field. Cardiovasc Res. 2009;82: 411-420
[36] Van Den Heuvel R, Leppens H, Nemethova G et al. Haemopietic cell proliferation in murine bone marrow cells exposed to extremely low frequency (ELF) electromagnetic fields. Toxicol In Vitro. 2001;15: 351–355
[37] Bai WF, Zhang MS, Huang H, Zhu HX, Xu WC. Effects of 50 Hz electromagnetic fields on human epidermal stem cells cultured on collagen sponge scaffolds. Int J Radiat Biol. 2012;88: 523-530
[38] Sun LY, Hsieh DK, Lin PC et al. Pulsed electromagnetic fields accelerate proliferation and osteogenic gene expression in human bone marrow mesenchymal stem cells during osteogenic differentiation. Bioelectromagnetics. 2010;31: 209–219
[39] Gaetani R, Ledda M, Barile L et al. Differentiation of human adult cardiac stem cells exposed to extremely lowfrequency electromagnetic field. Cardiovasc Res. 2009;82: 411–20
[40] Banas A, Teratani T, Yamamoto Y et al. Adipose tissue-derived mesenchymal stem cells as a source of humanhepatocytes. Hepatology. 2007;46:21-28
[41] Banas A, Teratani T, Yamamoto Y, et al. IFATS collection: in vivo therapeutic potential of human adipose tissue mesenchymal stem cells after transplantation into mice with liver injury. Stem Cells. 2008;26(10): 2705–2712
[42] Banas A, Teratani T, Yamamoto Y et al. Rapid hepatic fate specification of adipose-derived stem cells and their therapeutic potential for liver failure. J Gastroenterol Hepatol. 2009;24(1): 70-77
[43] Yamamoto Y, Banas A, Murata S et al. A comparative analysis of the transcriptome and signal pathways in hepatic differentiation of human adipose mesenchymal stem cells. FEBS J. 2008; 275(6):1260–1273
[44] Park JE, Seo YK, Yoon HH et al. Electromagnetic fields induce neural differentiation of human bone marrow derived mesenchymal stem cells via ROS mediated EGFR activation. Neurochem Int. 2013;62:418–424
[45] Cuccurazzu B. Leone L, Podda MV et al. Exposure to extremely low-frequency (50 Hz) electromagnetic fields enhance adult hippocampal neurogenesis in C57BL/6 mice. Exp Neurol. 2010; 226(1): 173-182
[46] Sherafat MA, Heibatollahi M, Mongabadi S et al. Electromagnetic field stimulation potentiates endogenous myelin repair by recruiting subventricular stem cells in an experimental model of white matter demyelination. J Mol Neurosci. 2012; 48(1): 144-153
[47] Bassett CA, Mitchell SN, Gaston SR. Pulsing electromagnetic field treatment in ununited fractures and failed arthrodeses. JAMA. 1982; 247:623-628
[48] Assiotis A, Sachinis NP, Chalidis BE. Pulsed electromagnetic fields for the treatment of tibial delayed unions and nonunions. A prospective clinical study and review of the literature. J Orthop Surg Res. 2012; 7: 24
[49] Chang K, Chang WH. Pulsed electromagnetic fields prevent osteoporosis in an ovariectomized female rat model: a prostaglandin E2-associated process. Bioelectromagnetics.2003; 24:189-198
[50] Rubin CT, McLeod KJ, Lanyon LE. Prevention of osteoporosis by pulsed electromagnetic fields. J Bone Joint Surg Am. 1989; 71: 411-417
[51] Sert C, Mustafa D, Duz MZ et al. The preventive effect on bone loss of 50-Hz, 1-mT electromagnetic field in ovariectomized rats. J Bone Miner Metab. 2002; 20: 345-349
[52] Jing D, Jing C, Wu Y et al. Pulsed Electromagnetic Fields Partially Preserve Bone Mass, Microarchitecture, and Strength by Promoting Bone Formation in Hindlimb-Suspended Rats. J Bone Miner Res. 2014; 29(10): 2250-2261
[53] Tabrah R, Hoffmeier M, Gilbert F Jr et al. Bone density changes in osteoporosis-prone women exposed to pulsed electromagnetic fields (PEMFs). J Bone Miner Res. 1990; 5: 437-442
[54] Bodamyali T, Bhatt B, Hughes FJ et al. Pulsed electromagnetic fields simultaneously induce osteogenesis and upregulate transcription of bone morphogenetic proteins 2 and 4 in rat osteoblasts in vitro. Biochem Biophys Res Commun. 1998; 250(2): 458-461
[55] Diniz P, Shomura K, Soejima K et al. Effects of pulsed electromagnetic field (PEMF) stimulation on bone tissue like formation are dependent on the maturation stages of the osteoblasts. Bioelectromagnetics. 2002; 23: 398-405
[56] Chang K, Hong-Shong Chang W, Yu YH et al. Pulsed electromagnetic field stimulation of bone marrow cells derived from ovariectomized rats affects osteoclast formation and local factor production. Bioelectromagnetics. 2004; 25:134-141
[57] De Mattei M, Caruso A, Pezzetti F et al. Effects of pulsed electromagnetic fields on human articular chondrocyte proliferation. Connect Tissue Res. 2001;42(4): 269-279
[58] Becker RO, Bassett CAL, Bachman CH. Bioelectric factors controlling bone structure. Frost H, editor. Boston, Little, Brown: Bone Biodynamics; 1964. pp. 209–32
[59] Yasuda I. Fundamental aspects of fracture treatment. J Kyoto Med SOC. 1953;4:392
[60] Otter M, Goheen S, Williams WS. Streaming potentials in chemically modified bone. J Orthop Res. 1988;6: 346-59
[61] Ross CL, Siriwardane M, Almeida-Porada G et al. The effect of low-frequency elektromagnetic field on human bone marrow stem/progenitor cell differentiation. Stem Cell Res. 2015;15: 96-108
[62] Schimmelpfeng J. Dertinger H. The action of 50 Hz magnetic and electric fields upon cell Proliferation and cyclic AMP content of cultured mammalian cell. Bioelectrochem Bioenerg 1993; 30: 143-50
[63] Dertinger H, Weiberzahn KF. Treatment of Psoriasis with Interferential Current – New Perspectives of electromagnetic therapy. Akt Dermatol 2002: 28: 165-169
[64] Ciombor DM, Aaron RK. The role of electrical stimulation in bone repair. Foot Ankle Clin. 2005; 10: 579–593
[65] Xu H, Zhang J, Lei Y et al. Low frequency pulsed electromagnetic field promotes C2C12 myoblasts proliferation via activation of MAPK/ERK pathway. Biochem Biophys Res Commun. 2016; 479(1): 97-102
[66] Li Y, Yan X, Liu J et al. Pulsed electromagnetic field enhances brain-derived neurotrophic factor expression through L-type voltage-gatged calcium channel- and Erk-dependent signalling pathways in neonatal rat dorsal root ganglion neurons. Neurochem Int. 2014; 75: 96-10
[67] Ehnert S, Falldorf K, Fentz AK et al. Primary human osteoblasts with reduced alkaline phosphatase and matrix mineralization baseline capacity are responsive to extremely low frequency pulsed electromagnetic feld exposure — Clinical implication possible. Bone Reports. 2015; 3: 48-56